Atomiteoria on kulkenut pitkän matkan muutaman tuhannen vuoden aikana. Alkaen 5. vuosisadalla eKr. Democrituksen teoriasta jakamattomista ”runkokerroista”, jotka ovat vuorovaikutuksessa keskenään, siirtyvät sitten Daltonin atomimalliin 18-luvulla ja kypsyvät sitten 20-luvulla löydettäessä subatomisia hiukkasia ja kvantiteoriaa, löytömatka on ollut pitkä ja mutkikas.
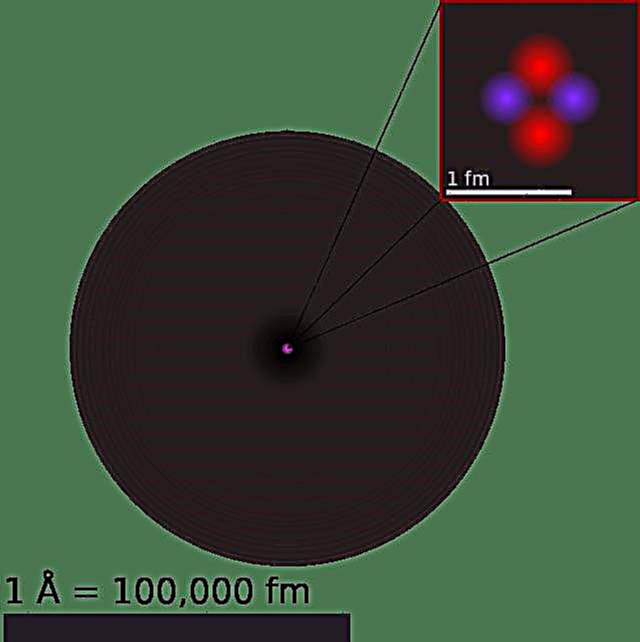
Todennäköisesti yksi tärkeimmistä virstanpylväistä matkalla on ollut Bohrin atomimalli, jota kutsutaan joskus Rutherford-Bohr-atomimalliksi. Tanskalaisen fyysikon Niels Bohrin vuonna 1913 ehdottama malli kuvaa atomia pienenä, positiivisesti varautuneena ytimenä, jota ympäröivät elektronit, jotka kulkevat ympyrän kiertoradalla (määritelty niiden energiatasoilla) keskuksen ympäri.
Atomiteoria 1800-luvulle:
Varhaisimmat tunnetut esimerkit atomiteoriasta ovat peräisin muinaisesta Kreikasta ja Intiasta, joissa filosofit, kuten Democritus, postuloivat, että kaikki aine koostui pienistä, jakamattomista ja tuhoutumattomista yksiköistä. Termi ”atomi” kehitettiin antiikin Kreikassa, ja se johti ajatuskouluun, joka tunnetaan nimellä “atomismi”. Tämä teoria oli kuitenkin enemmän filosofinen käsite kuin tieteellinen.
Vasta atomien teoriaa artikuloitiin vasta 1800-luvulla tieteelliseksi asiaksi, kun ensimmäiset todisteisiin perustuvat kokeet tehtiin. Esimerkiksi 1800-luvun alkupuolella englantilainen tutkija John Dalton käytti atomin käsitettä selittääkseen miksi kemialliset elementit reagoivat tietyillä havaittavissa olevilla ja ennustettavilla tavoilla. Kaasuihin liittyvien kokeilujen avulla Dalton kehitti edelleen niin kutsuttua Daltonin atomiteoriaa.
Tämä teoria laajeni massan ja tiettyjen mittasuhteiden keskustelulakeihin ja tuli viiteen oletukseen: elementit ovat puhtaimmassa tilassaan hiukkasista, joita kutsutaan atomeiksi; tietyn alkuaineen atomit ovat kaikki samoja aina viimeiseen atomiin asti; Eri elementtien atomit voidaan erottaa toisistaan niiden atomipainojen perusteella; alkuaineiden atomit yhdistyvät kemiallisten yhdisteiden muodostamiseksi; atomeja ei voida luoda tai tuhota kemiallisessa reaktiossa, vain ryhmittely muuttuu koskaan.
Elektronin löytö:
1800-luvun lopulla tutkijat alkoivat myös teorioida, että atomi koostui useammasta kuin yhdestä perusyksiköstä. Useimmat tutkijat uskoivat kuitenkin, että tämä yksikkö olisi pienimmän tunnetun atomin - vedyn - kokoinen. 1800-luvun loppuun mennessä tämä muuttuisi dramaattisesti Sir Joseph John Thomsonin kaltaisten tutkijoiden tekemän tutkimuksen ansiosta.
Thomson havaitsi, että katodisäteputkia (tunnetaan Crookes 'Tube) käyttävien kokeiden avulla katodisäteitä voidaan ohjata sähkö- ja magneettikentän avulla. Hän päätteli, että sen sijaan, että ne koostuisivat valosta, ne koostuivat negatiivisesti varautuneista hiukkasista, jotka olivat 1 kertaa kertaa pienemmät ja 1800 kertaa kevyemmät kuin vety.

Tämä kumosi käytännössä käsityksen, että vetyatomi oli pienin aineyksikkö, ja Thompson meni pidemmälle ehdottaakseen atomien jakautumista. Selittääkseen atomin kokonaisvarauksen, joka koostui sekä positiivisista että negatiivisista varauksista, Thompson ehdotti mallia, jolla negatiivisesti varautuneet “runkokerrat” jakautuisi yhtenäiseen positiivisen varauksen mereen - joka tunnetaan nimellä Plum Pudding Model.
Näitä hiukkasia kutsutaan myöhemmin "elektroneiksi", jotka perustuvat englantilais-irlantilaisen fyysikon George Johnstone Stoneyn vuonna 1874 ennustamaan teoreettiseen hiukkasiin. Ja siitä syntyi Plum Pudding -malli, nimeltään, koska se muistutti läheisesti Englannin autiomaa, joka koostuu luumukakku ja rusinat. Konsepti esiteltiin maailmalle Ison-Britannian maaliskuun 1904 painos Philosophical Magazine, laajalti suosiota.
Rutherford-malli:
Myöhemmät kokeet paljastivat lukuisia tieteellisiä ongelmia Plum Pudding -mallin kanssa. Ensinnäkin oli ongelma osoittaa, että atomilla oli tasainen positiivinen taustavaraus, jota kutsuttiin nimellä “Thomson-ongelma”. Viisi vuotta myöhemmin mallia hylkäsivät Hans Geiger ja Ernest Marsden, jotka tekivät sarjan kokeita, joissa käytettiin alfahiukkasia ja kultafoliota eli aka. "kultafolion kokeilu".
Tässä kokeessa Geiger ja Marsden mittasivat alfahiukkasten sirontakuvion fluoresoivalla seulalla. Jos Thomsonin malli olisi oikein, alfahiukkaset kulkisivat folion atomirakenteen esteettä. Kuitenkin, he huomauttivat sen sijaan, että vaikka suurin osa ampui suoraan läpi, jotkut heistä olivat hajallaan eri suuntiin, kun taas jotkut menivät takaisin lähteen suuntaan.

Geiger ja Marsden päättelivät, että hiukkaset olivat törmänneet sähköstaattiseen voimaan, joka on paljon suurempi kuin mitä Thomsonin malli sallii. Koska alfahiukkaset ovat vain heliumydimiä (jotka ovat positiivisesti varautuneita), tämä tarkoitti, että atomin positiivinen varaus ei hajaantunut laajasti, vaan keskittyi pieneen tilavuuteen. Lisäksi se, että nuo hiukkaset, joita ei taiputtu, läpäisivät esteettä, tarkoittivat, että nämä positiiviset tilat erotettiin valtavien tyhjän tilan kuilujen avulla.
Vuoteen 1911 mennessä fyysikko Ernest Rutherford tulkitsi Geiger-Marsden-kokeita ja hylkäsi Thomsonin mallin atomista. Sen sijaan hän ehdotti mallia, jossa atomi koostui pääosin tyhjästä tilasta, jonka kaikki positiiviset varaukset olivat keskittyneet sen keskukseen hyvin pienessä tilavuudessa, jota ympäröi elektronipilvi. Tätä kutsuttiin atomin Rutherford-malliksi.
Bohr-malli:
Myöhemmät Antonius Van den Broekin ja Niels Bohrin kokeilut paransivat mallia edelleen. Vaikka Van den Broek ehdotti, että elementin atominumero on hyvin samanlainen kuin sen ydinvaraus, jälkimmäinen ehdotti atomin aurinkokunnan kaltaista mallia, jossa ydin sisältää positiivisen varauksen atomimäärän ja jota ympäröi sama elektronien lukumäärä kiertoradalla (tunnetaan myös nimellä Bohr-malli).
Lisäksi Bohrin malli tarkensi tiettyjä Rutherford-mallin osia, jotka olivat ongelmallisia. Näihin sisältyi klassisesta mekaniikasta johtuvia ongelmia, jotka ennustivat elektroneiden vapauttavan sähkömagneettista säteilyä ytimen kiertäessä. Energian menetyksen vuoksi elektronin olisi pitänyt kääntyä nopeasti sisäänpäin ja romahtaa ytimeen. Lyhyesti sanottuna tämä atomimalli tarkoitti, että kaikki atomit olivat epävakaita.

Malli ennusti myös, että elektronien kääntyessä sisäänpäin, niiden emissio nousee nopeasti taajuudella kiertoradan pienentyessä ja nopeammin. Kuitenkin 1800-luvun lopun kokeet sähköpurkauksilla osoittivat, että atomit lähettävät sähkömagneettista energiaa vain tietyillä erillisillä taajuuksilla.
Bohr ratkaisi tämän ehdottamalla, että elektronit kiertävät ydintä tavoilla, jotka ovat yhdenmukaisia Planckin säteilyn kvantiteorian kanssa. Tässä mallissa elektronit voivat miehittää vain tietyt sallitut kiertoradat tietyllä energialla. Lisäksi ne voivat saada ja menettää energiaa vain hyppäämällä sallitusta kiertoradalta toiselle, absorboimalla tai lähettämällä prosessissa sähkömagneettista säteilyä.
Nämä kiertoradat liittyivät tiettyihin energioihin, joihin hän viittasi energiakuoret tai energiatasot. Toisin sanoen atomin sisällä olevan elektronin energia ei ole jatkuvaa, vaan ”kvantisoitu”. Nämä tasot on siis merkitty kvanttilukuilla n (n = 1, 2, 3 jne.), jonka hän väitti voivan määrittää käyttämällä Ryberg-kaavaa - sääntö, jonka ruotsalainen fyysikko Johannes Ryberg muotoili vuonna 1888 kuvaamaan monien kemiallisten elementtien spektriviivojen aallonpituudet.
Bohr-mallin vaikutus:
Vaikka Bohrin malli osoittautui tietyssä suhteessa uraauurtavaksi - Rybergin vakion ja Planckin vakion (aka. Kvanttiteorian) yhdistäminen Rutherford-malliin -, se kärsi joistakin puutteista, joita myöhemmät kokeilut osoittaisivat. Ensinnäkin se oletti, että elektronilla on sekä tunnettu säde että kiertorata, jota Werner Heisenberg kumoaa kymmenen vuotta myöhemmin epävarmuusperiaatteellaan.
Lisäksi, vaikka se oli hyödyllinen ennakoimaan elektronien käyttäytymistä vetyatomeissa, Bohrin malli ei ollut erityisen hyödyllinen ennustaessa suurempien atomien spektriä. Näissä tapauksissa, joissa atomilla on useita elektroneja, energian tasot eivät olleet yhdenmukaisia sen kanssa, mitä Bohr ennusti. Malli ei myöskään toiminut neutraalien heliumiatomien kanssa.
Bohr-malli ei myöskään voinut ottaa huomioon Zeeman-ilmiötä, ilmiötä, jonka hollantilaiset fyysikot Pieter Zeeman havaitsivat vuonna 1902, jossa spektriviivat jaetaan kahteen tai useampaan ulkoisen staattisen magneettikentän läsnä ollessa. Tämän vuoksi Bohrin atomimallissa yritettiin tehdä useita tarkennuksia, mutta myös nämä osoittautuivat ongelmalliseksi.
Loppujen lopuksi tämä johtaisi siihen, että Bohrin malli korvataan kvantiteorialla - Heisenbergin ja Erwin Schrodingerin työn mukaisesti. Siitä huolimatta Bohrin malli on edelleen käyttökelpoinen ohjeellisena työkaluna opiskelijoiden tutustuttamiseksi nykyaikaisempiin teorioihin - kuten kvanttimekaniikkaan ja valenssikuoren atomimalliin.
Se osoittautuu myös tärkeäksi virstanpylväksi kehitettäessä hiukkasfysiikan standardimallia, mallia, jolle on tunnusomaista ”elektronipilvet”, alkuainepartikkelit ja epävarmuus.
Olemme kirjoittaneet monia mielenkiintoisia artikkeleita atomiteoriasta täällä Space Magazine. Tässä on John Daltonin atomimalli, mikä on luumujen pudotusmalli, mikä on elektronipilvomalli, kuka oli Democritus? Ja mitkä ovat atomin osia?
Astronomy Cast -teoksessa on myös joitain jaksoja aiheesta: Jakso 138: Kvanttimekaniikka, Jakso 139: Energiatasot ja spektrit, Jakso 378: Rutherford ja atomit ja jakso 392: Vakiomalli - Johdanto.
Lähteet:
- Niels Bohr (1913) ”Atomien ja molekyylien perustamisesta, osa I”
- Niels Bohr (1913) ”Atomien ja molekyylien muodostamisesta, osa II, vain yhden ytimen sisältävät järjestelmät”
- Encyclopaedia Britannica: Borh Atomic -malli
- Hyperfysiikka - Bohr-malli
- Tennessee University, Knoxville - Borhin malli
- Toronton yliopisto - Atomin Bohr-malli
- NASA - Kuvittele maailmankaikkeus - Tausta: atomit ja valoenergia
- Tietoja koulutuksesta - Bohr-malli atomista